硝酸汞
化合物
硝酸汞(化學式:Hg(NO3)2)是一種主要用於實驗室的化學試劑。
| 硝酸汞 | |
|---|---|
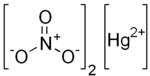
| |

| |
| IUPAC名 Mercury dinitrate Mercury(II) nitrate | |
| 別名 | 硝酸高汞、硝酸汞(Ⅱ) |
| 識別 | |
| CAS號 | 10045-94-0(無水物) 7783-34-8(一水合物) |
| PubChem | 16683796 |
| ChemSpider | 23247 |
| SMILES |
|
| InChI |
|
| InChIKey | ORMNPSYMZOGSSV-UHFFFAOYAS |
| UN編號 | 1625 |
| EINECS | 233-152-3 |
| RTECS | OW8225000 |
| 性質 | |
| 化學式 | Hg(NO3)2 |
| 莫耳質量 | 324.606 g·mol⁻¹ |
| 外觀 | 無色至淡黃色晶體或白色粉末 |
| 密度 | 4.3 g/cm3(一水合物) |
| 熔點 | 79 °C(一水合物) 145 °C(半水合物熔融分解) |
| 溶解性 | 可溶於水、硝酸,不溶於乙醇 |
| 危險性 | |
| 警示術語 | R:R26/27/28, R33, R50/53 |
| 安全術語 | S:S1/2, S13, S28, S45, S60, S61 |
| MSDS | ICSC 0980 |
| 歐盟編號 | 080-002-00-6 |
| 歐盟分類 |   劇毒品(T+) 對環境有害(N) |
| NFPA 704 | |
| 閃點 | 不可燃 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
性質
編輯硝酸汞是無色或白色透明結晶或白色粉末,有較強的潮解性。劇毒。易溶於水、稀硝酸、丙酮,難溶於乙醇。有半水和一水兩種水合物,其中以半水合物最為常見。半水合物加熱時脫水生成鹼式鹽 Hg3O2(NO3)2,緩緩加熱時生成氧化汞,強熱時則生成汞、二氧化氮和氧氣。
在溶液中硝酸汞幾乎完全以未離解分子的形式存在,在水中迅速發生水解,生成 Hg3O2(NO3)2·2H2O 的沉澱。在 Hg2+-NO3− 的水溶液體系中,lg K1 約為0.3,同時存在 Hg(NO3)3− 和 Hg(NO3)42−。乙醇溶液中,硝酸汞與 NMe4NO3 反應得到固態的 (NMe4)2[Hg(NO3)4],其中的汞為八配位,四個 NO3− 均以雙牙基的方式與汞進行配位。
將銅絲放置於硝酸汞的溶液中,會發生置換,生成藍色的硝酸銅溶液和金屬汞。雖說銅的金屬活動性排在氫之後,但和硝酸汞反應的時候仍會產生少量黃色氧化汞沉澱。
製備
編輯由濃硝酸和金屬汞生成,副產物是一氧化氮或二氧化氮,副產物的種類視硝酸的濃度而不同。根據不同條件可從硝酸汞溶液中得到含半分子水或一分子水的水合物。
無水硝酸汞可通過氧化汞和四氧化二氮的反應製取。首先生成加合物 Hg(NO3)2·N2O4,然後在真空中稍加熱脫去 N2O4 即得到無水硝酸汞。
用途
編輯參見
編輯參考資料
編輯- 呂雲陽,王文紹,劉頌禹,季振平.《無機化學叢書》第六卷 鹵素、銅分族、鋅分族.北京:科學出版社,1998年.頁848.書號 03-003647-6.
